Na tabela periódica, os elementos estão dispostos em ordem
crescente de número atômico.
Cada fila vertical denomina-se de família ou grupo.
(existem 18) - Os elementos de uma mesma família apresentam propriedades
químicas semelhantes, ou seja, possuem a mesma configuração eletrônica na
última camada.
Cada fila horizontal denomina-se período.
(existem 7) - indicam a quantidade de camadas ou níveis de energia na
configuração eletrônica dos elementos. Assim, se o potássio (K) localiza-se no
quarto período, ele possui quatro camadas de energia (K L M N).
Os gases nobres são os elementos químicos
com 8 elétrons na última camada em sua distribuição
eletrônica. (eles possuem uma relativa dificuldade de combinação com outros
átomos porque são pouco reativos.)
Os Lantanídeos também são conhecidos como terra
raras. Junto com os actinídeos, constituem os elementos
de transição interna.
Os grupos 1,2,13,14,15,16,17 e 18 ou família A, são chamados
de representativos. Pois o subnível mais energético da camada de valência é s
ou p.
Os grupos 3,4,5,6,7,8,9,10,11 e 12 são chamados de
transição, pois o subnível mais energético da penúltima camada é d.
Mas, se o subnível mais energético
da antepenúltima camada é f, sao chamados de transição
interna.
Com o aumento do número atômico ao longo do grupo a
eletronegatividade decresce e o raio atômico cresce.
Observação: O hidrogênio está
localizado na família 1A, somente porque possui um elétron na última camada. Na
verdade, ele não é um metal alcalino, pois possui propriedades químicas
diferentes dos demais elementos dessa família.
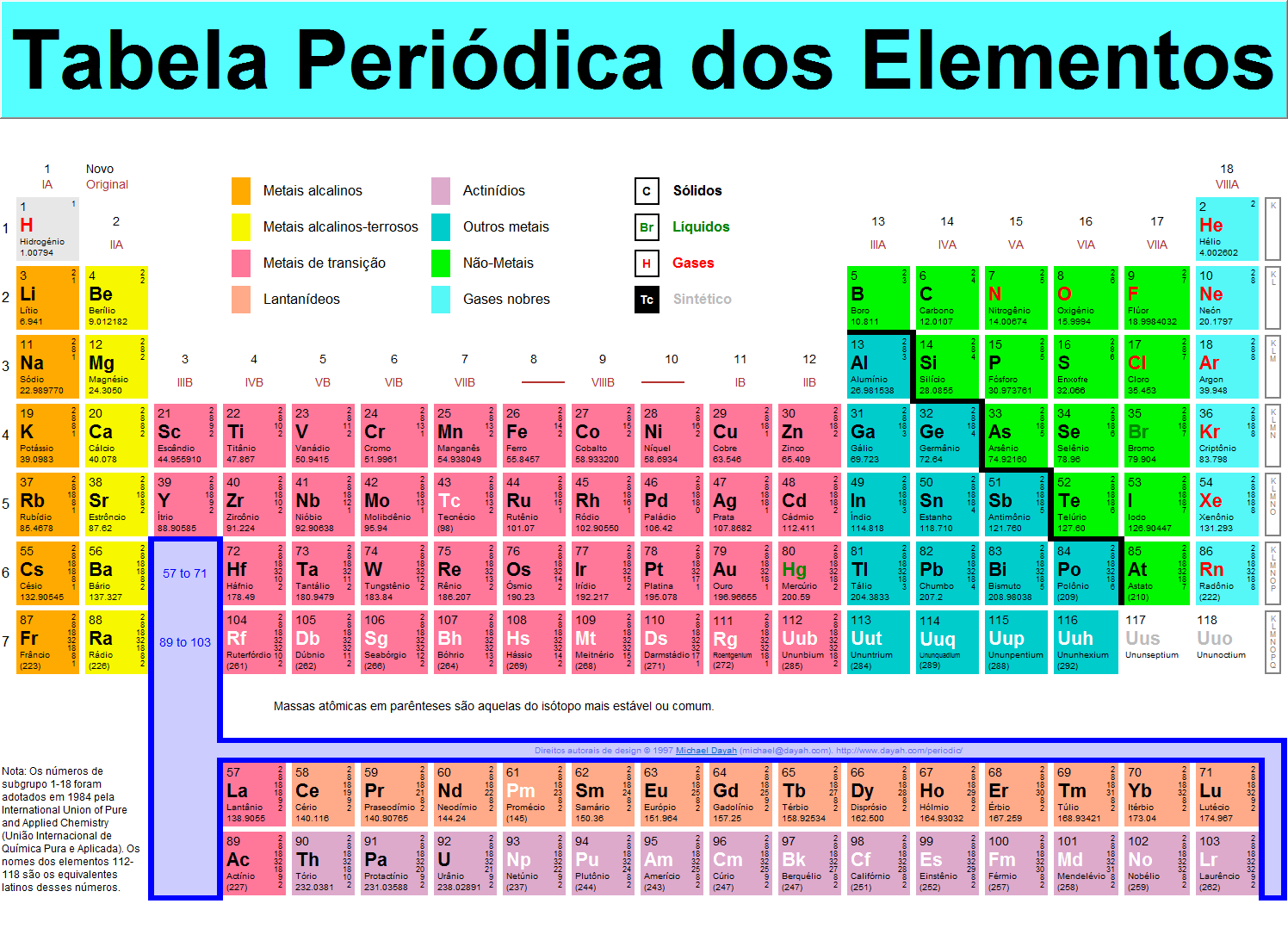
Famílias
I like your blog :D
ResponderExcluirgostei muito mesmo
ResponderExcluirOs elementos de transição simples apresentam subnível ...... Da penúltima camada como o subnível mais energético. Me ajudem
ResponderExcluir